Dreifache negative Brustkrebs exprimieren Rezeptoren für LHRH und sind potentielle therapeutische Ziele für zytotoxische LHRH-Analoga, AEZS 108
Wirkung der Behandlung mit AEZS 108 auf das Tumorwachstum in vivo
In dem ersten Experiment inhibierten 3 Injektionen von zytotoxischem LHRH-Analoga AEZS-108, (1,45 mg / kg) , das Wachstum der Tumorzellen MDA-MB-231 nach 14 Tagen im Vergleich zur Kontrollgruppe. Die hemmende Wirkung von AEZS-108 unterscheidete sich signifikant im Gegensatz zu der Kontrollgrupe und DOX (1,45 mg/kg) bis zum Ende der Studie (Tag 28). Achtundzwanzig Tage nach der Injektion von AEZS-108 wurde das Tumorvolumen um 59% im Vergleich zu Kontrollgrupe reduziert . Eine äquimolare Dosis des zytotoxischen Radikals, DOX allein, zeigte keine signifikanten wachstumshemmenden Effekte (Fig. 6).
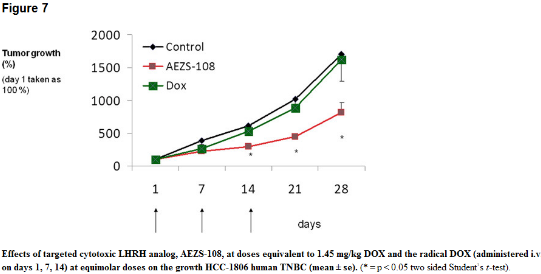
Im zweiten Experiment unterdrückte die Verabreichung von 3 Dosen zytotoxischer LHRH-analoger AEZS-108 (1,45 mg / kg) die Proliferation von humanem Tumorzellen HCN-1806 signifikant. Die Tumorvolumina waren vom Behandlungstag 15 bis zum Ende des Experiments signifikant niedriger. Achtundzwanzig Tage nach der Verabreichung von AEZS-108 wurde das Tumorvolumen um 52% reduziert. Eine äquimolare Dosis des zytotoxischen Radikals, DOX alleine, hatte keine signifikanten Auswirkungen auf irgendwelche Tumorwachstumsparameter (Fig. 7).
Diskussion
AEZS-108 wurde bereits in Nacktmäusen mit Xenotransplantaten verschiedener menschlicher Brustkrebslinien einschließlich der LHRH-Rezeptor-positiven und Doxorubicin-resistenten menschlichen MX-1-Brustkrebs-Zelllinie getestet. AEZS-108 hemmte signifikant das Wachstum dieser MX-1-Zellen, während das unkonjugierte Doxorubicin unwirksam war. Auch die Expression von mRNA für HER-2 und HER-3 sowie die Werte von HER-2 und HER-3-Proteinen wurde durch die Behandlung mit AEZS-108 signifikant reduziert. Toxische Nebenwirkungen wie Leukopenie waren bei Tieren, die mit AEZS-108 im Vergleich zu denen mit unkonjugiertem Doxorubicin behandelt wurden, weniger ausgeprägt auf .
Die Behandlung von dreifach negativem LHRH-Rezeptor-positiven MDA-MB-231, HCC1806 und HCC1937 menschlichen Brustkrebszellen mit AEZS-108 führte zu einem apoptotischen Zelltod, dies wurde anhand der Caspase-3-Spaltung bestätigt. Die Antitumorwirkungen wurden in vivo bestätigt, da AEZS-108 das Wachstum der dreifach negativen Brustkrebserkrankungen HCC1806 und MDA-MB-231 signifikant inhibierte, die in nackte Mäuse ohne offensichtliche toxische Nebenwirkungen exprimiert sind.
Quelle: PMID: 25410881
|
Angehängte Grafik:
xx.png (verkleinert auf 94%)